HARP現象の研究
— HARP現象:Nature advertisement feature (PDF)/(URL)
異分野融合研究のニーズ
がんは我が国の死因の第1位。現在1次治療は進んでいるが、再発が問題となっている。
研究の背景ですが、がんは我が国の死因の第1位で、克服すべき疾患です。①現在外科手術、薬物治療、放射線など1次治療は進んでいますが、再発が問題となっています。②がんには少数の治療が効かないがん幹細胞があり、再発の原因となります。③がん組織はがん幹細胞が分化しながら構成されていますが、がん幹細胞は少数で性質も変化するため、診断法、治療法はなく、がん幹細胞を迅速に見つける方法が高い社会のニーズとなっています。
- 国内がん死亡者数38.1万人(2021年)

- がん幹細胞は再発の原因となる
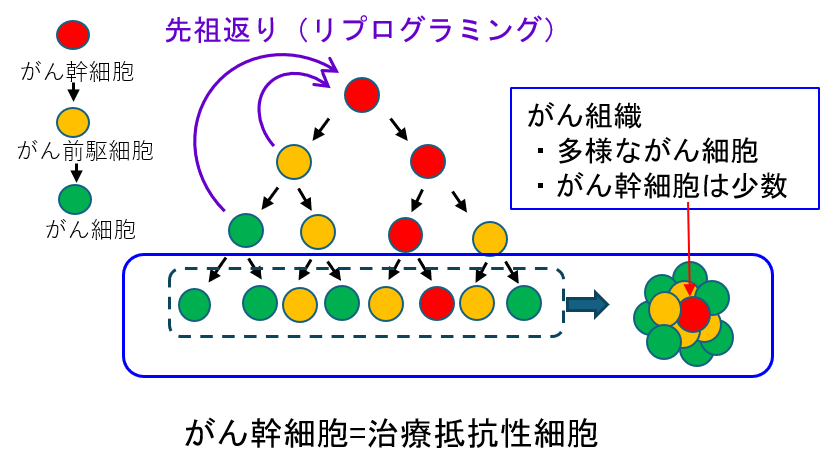
- がん幹細胞が分化しながらがん組織が構成される
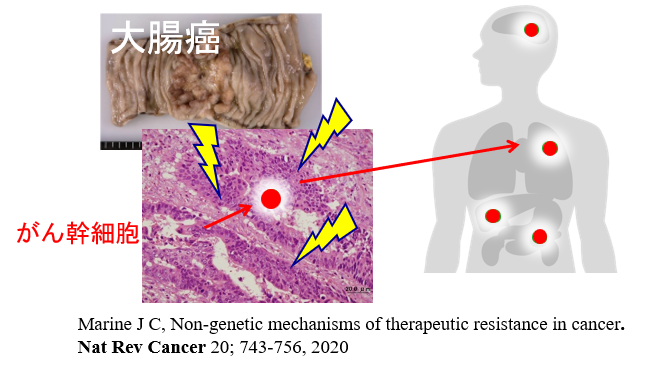
がん医療の問題点:がん幹細胞は少量で、性質が変化するため実用化されている検出法、診断法、治療法はない。
高い社会のニーズ がん幹細胞を迅速に見つける方法が必要
研究の発端となる発見
ハイドロゲルががん幹細胞を迅速に創出する事を発見:HARP現象
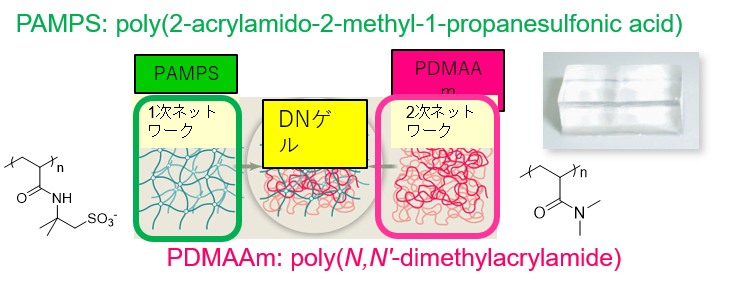
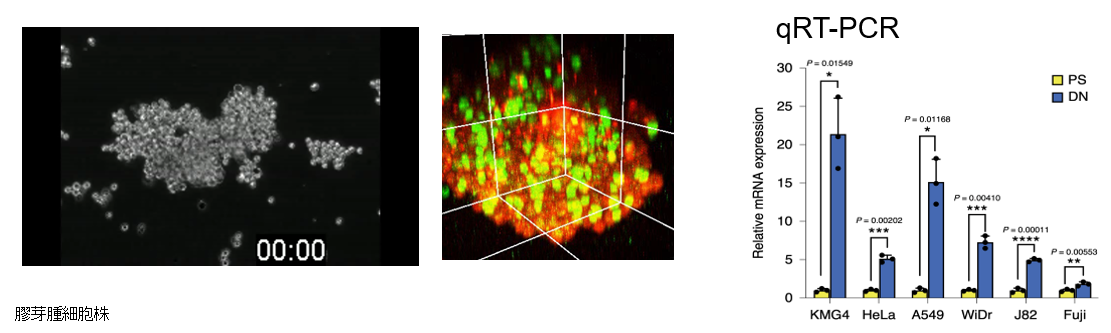
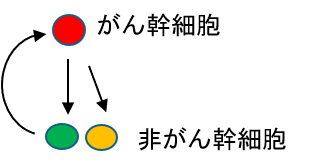
研究の発端となる発見ですが、①に示すように、我々はアクリルアミドを基盤とした2種類のネットワークを有するダブルネットワークハイドロゲルが短時間でがん幹細胞を創り出すことを見いだしました。②DNゲルに細胞をまくと急速にスフェロイドが形成され、がん幹細胞が創られます。緑は幹細胞マーカーSox2の蛍光抗体法での発現です。③は模式図ですが、赤いがん幹細胞が増えるのではなく、緑や黄色のがん細胞が先祖返りをして、赤のがん幹細胞となります。我々は、この現象をHydrogel activated reprogrammingハープ現象と名付けました。
- 2つの成分から構成されるダブルネットワーク(DN)ゲル
- ゲルによるSpheroid形成とがん幹細胞マーカーの発現
- HARP現象の概要


Suzuka, et al. Nat Biomed Eng, 5, 2021.
命名:ゲルによる迅速ながん幹細胞創出をHARP(Hydrogel Activated ReProgramming )現象と命名
異分野融合研究の概要
バイオマテリアルを利用して細胞の運命を変える
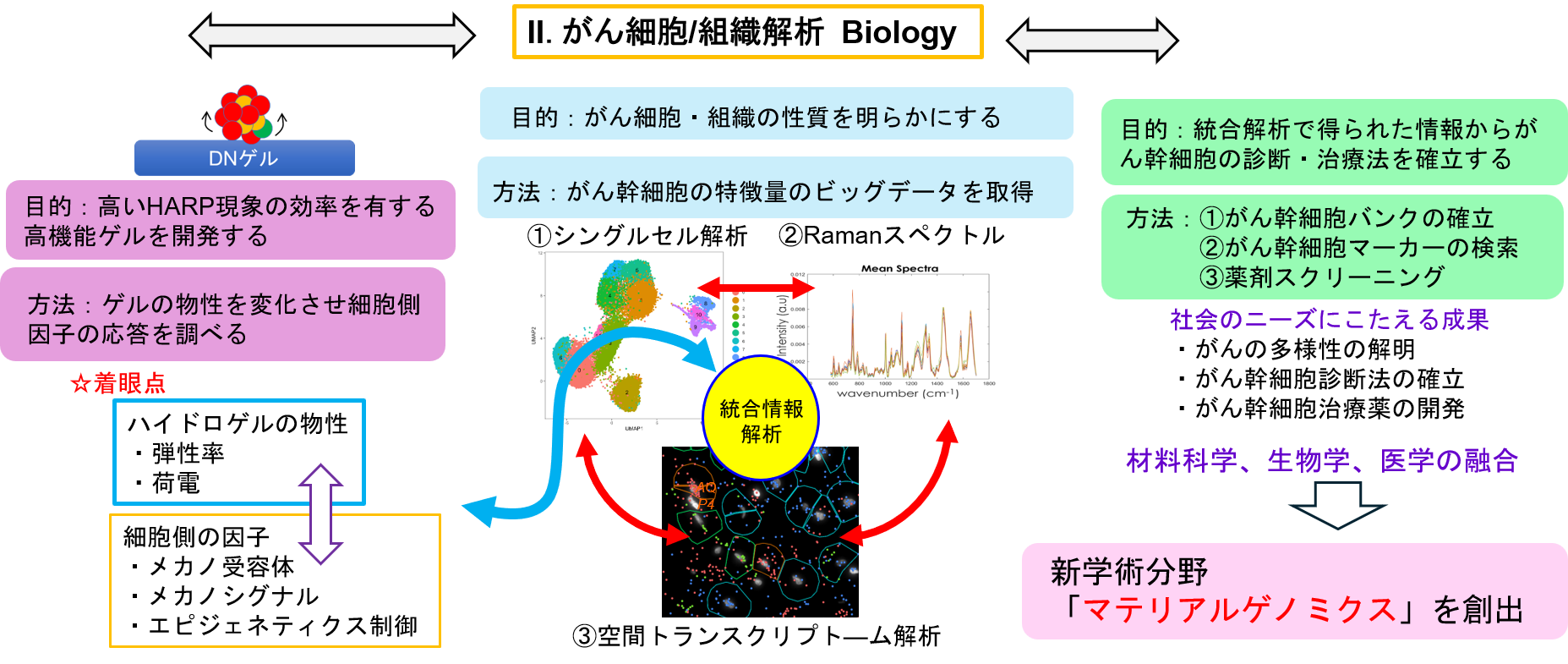
研究の概要です。我々の研究の基軸は「バイオマテリアルを利用して細胞の運命を変える」ことにあります。研究は3つの領域からなり、①ゲル開発、では、ゲルの物性を変えることで、細胞内のしくみを解明して、高いがん幹細胞創出高率を有するゲルを開発します。②「がん細胞/組織解析」では、ゲルを利用してがんの性質を明らかにします。方法は、シングルセル解析、Ramanスペクトル、空間トランスクリプト―ム解析を実施して、数十万の細胞から数万遺伝子の情報、スペクトル情報などのビッグデータを取得して、ゲルの物性パラメータをあわせて統合的に解析します。この結果を、「診断治療研究」の場では、実際の患者検体を用いて検証し、癌の多様性の解明、がん幹細胞の診断法・治療法を確立します。この一連の研究は、材料科学、生物学、医学の異分野融合研究の成果となり、新学術分野「マテリアルゲノミクス」を創出します。
論文発表
ハイドロゲルに関する教室オリジナル論文
- Hashimoto D, Semba S, Tsuda M, Kurokawa T, Kitamura N, Yasuda K, Gong J P, and Tanaka S. Integrin α4 mediates ATDC5 cell adhesion to negatively charged synthetic polymer hydrogel leading to chondrogenic differentiation. Biochem Biophys Res Commun, 528, 120-126, 2020.
- Semba S, Kitamura N, Tsuda M, Goto K, Kurono S, Ohmiya Y, Kurokawa T, Gong J P, Yasuda K, and Tanaka S. Synthetic PAMPS gel induces chondrogenic differentiation of ATDC5 cells via a novel protein reservoir function. J Biomed Mater Res A, 1-11, 2020.
- Suzuka J, Tsuda M, Wang L, Kohsaka S, Kishida K, Semba S, Sugino H, Aburatani S, Frauenlob M, Kurokawa T, Kojima S, Ueno T, Ohmiya Y, Mano H, Yasuda K, Gong J P, and Tanaka S. Rapid reprogramming of tumour cells into cancer stem cells on double-network hydrogels. Nat Biomed Eng, 5, 914-925, 2021.
- Ferdous Z, Clément J E, Gong J P, Tanaka S, Komatsuzaki T, and Tsuda M. Geometrical analysis identified morphological features of hydrogel-induced cancer stem cells in synovial sarcoma model cells. Biochem Biophys Res Commun, 642, 41-49, 2023.
- Tanikawa S, Ebisu Y, Sedlačík T, Semba S, Nonoyama T, Kurokawa T, Hirota A, Takahashi T, Yamaguchi K, Imajo M, Kato H, Nishimura T, Tanei Z I, Tsuda M, Nemoto T, Gong J P, and Tanaka S. Engineering of an electrically charged hydrogel implanted into a traumatic brain injury model for stepwise neuronal tissue reconstruction. Sci Rep, 13, 2233, 2023.
- Kato-Shinomiya M, Sugino H, Wang L, Saito Y, He J, Tanei Z I, Oda Y, Tanikawa S, Tanino M, Gong J P, Tsuda M, and Tanaka S. SLC13A5 plays an essential role in the energy shift to oxidative phosphorylation in cisplatin-resistant mesothelioma stem cells. Pathol Int, 75, 151-165, 2025.
- Nie Y, Mu Q, Sun Y, Ferdous Z, Wang L, Chen C, Nakajima T, Gong J P, Tanaka S, and Tsuda M. Mechanochemistry-Induced Universal Hydrogel Surface Modification for Orientation and Enhanced Differentiation of Skeletal Muscle Myoblasts. ACS Appl Bio Mater, 2025.
- Sun Y, Nie Y, Wang L, Gong J P, Tanaka S, and Tsuda M. Tumor-mimetic hydrogel stiffness regulates cancer stemness properties in H-Ras-transformed cancer model cells. Biochem Biophys Res Commun, 743, 151163, 2025.
- Sawai S, Oda Y, Saito Y, Kuwabara T, Wang L, Tanei Z I, Hirabayashi S, Tsuda M, Gong J P, Manabe A, and Tanaka S. Analysis of synthetic polymer hydrogel-based generation of leukemia stem cells. Biochem Biophys Res Commun, 744, 151149, 2025.
- Aoki Y, Wang L, Tsuda M, Saito Y, Kubota T, Oda Y, Hirano S, Gong J P, and Tanaka S. Hydrogel PCDME creates pancreatic cancer stem cells in OXPHOS metabolic state with TXNIP elevation. Biochem Biophys Res Commun, 751, 151416, 2025.
ハイドロゲルに関する共同研究論文
- Goto K, Kimura T, Kitamura N, Semba S, Ohmiya Y, Aburatani S, Matsukura S, Tsuda M, Kurokawa T, Gong J P, Tanaka S, and Yasuda K. Synthetic PAMPS gel activates BMP/Smad signaling pathway in ATDC5 Cells, which plays a significant role in the gel-induced chondrogenic differentiation. J Biomed Mater Res A, 734-746, 2015.
- Frauenlob M, King D R, Guo H, Ishihara S, Tsuda M, Kurokawa T, Haga H, Tanaka S, and Gong J P. Modulation and Characterization of the Double Network Hydrogel Surface-Bulk Transition. Macromolecules, 52, 6704-6713, 2019.
- Huang J, Frauenlob M, Shibata Y, Wang L, Nakajima T, Nonoyama T, Tsuda M, Tanaka S, Kurokawa T, and Gong J P. Chitin-Based Double-Network Hydrogel as Potential Superficial Soft-Tissue-Repairing Materials. Biomacromolecules, 21, 4220-4230, 2020.
- Nonoyama T, Wang L, Tsuda M, Suzuki Y, Kiyama R, Yasuda K, Tanaka S, Nagata K, Fujita R, Sakamoto N, Kawasaki N, Yurimoto H, and Gong J P. Isotope Microscopic Observation of Osteogenesis Process Forming Robust Bonding of Double Network Hydrogel to Bone. Adv Healthc Mater, e2001731, 2020.
- Kaibara T, Wang L, Tsuda M, Nonoyama T, Kurokawa T, Iwasaki N, Gong J P, Tanaka S, and Yasuda K. Hydroxyapatite-hybridized double-network hydrogel surface enhances differentiation of bone marrow-derived mesenchymal stem cells to osteogenic cells. J Biomed Mater Res A, 2021.
- Mu Q, Cui K, Wang Z J, Matsuda T, Cui W, Kato H, Namiki S, Yamazaki T, Frauenlob M, Nonoyama T, Tsuda M, Tanaka S, Nakajima T, and Gong J P. Force-triggered rapid microstructure growth on hydrogel surface for on-demand functions. Nat Commun, 13, 6213, 2022.
